Источники кислорода для окисления примесей
Для окисления примесей мартеновской ванны при работе печи скрап-процессом необходимо кислорода ~3,5%, а при работе скрап-рудным процессом ~8% от массы металла. Основными источниками кислорода в мартеновской печи являются специально присаживаемые твердые окислители (железная руда, агломерат и т. д.), вдуваемый газообразный кислород и атмосфера печи. Следует отметить, что в связи с окислительным характером атмосферы в рабочем пространстве печи (содержание СO2 составляет 7—10%, а H2O 10—20%) она является в отличие от печной атмосферы других сталеплавильных агрегатов существенным источником кислорода для окислительных процессов в ванне. Этим объясняются окислительные свойства шлака, который является передаточным звеном кислорода в системе печная атмосфера—шлак—жидкий металл.
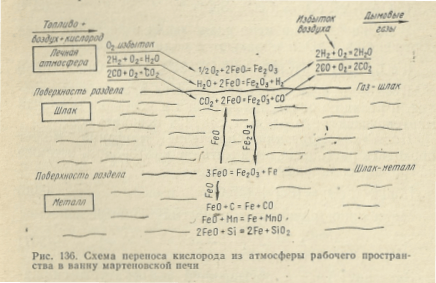
Схема передачи, кислорода из газовой атмосферы в металл приведена на рис. 136. На поверхности раздела газ—шлак протекают процессы окисления FeO до Fe2O3, который перемещается к поверхности раздела шлак-— металл и взаимодействует с железом по реакции
(Fe2O3) + [Fe] = 3(FeO). (201)
Образующийся оксид FeO взаимодействует с примесями металла на границе раздела металл — шлак или растворяется в металле:
(FeO) = [Fe] + [О]. (202)
В соответствии с законом распределения увеличение содержания оксидов железа в шлаке приводит к увеличению перехода кислорода в металл, одновременно возрастает и количество железа, переходящее из шлака в металл. При повышенном расходе чугуна увеличивается расход железной руды для окисления примесей и выход жидкого металла вследствие восстановления железа твердого окислителя. По этой, причине при скрап-рудном процессе наблюдается максимальный выход жидкого металла относительно загружаемой металлической шихты по сравнению с другими сталеплавильными агрегатами, что является несомненным преимуществом скрап-рудного мартеновского процесса.
Газообразный кислород, непосредственно вдуваемый в ванну, взаимодействует с примесями металла с положительным тепловым эффектом, что улучшает тепловой баланс процесса и позволяет ускорить нагрев металла.
Окисление кремния
При основном мартеновском процессе кремний полностью окисляется в период плавления, когда температура ванны еще относительно низка:
[Si] + 2[О] = (SiO2) + 331 кДж (78990 кал). (203)
Окисление кремния протекает с выделением тепла, что особенно важно в начальные периоды плавки, когда ванна недостаточно нагрета.
В начале плавления известняк не успевает раствориться в шлаке и образующийся кремнезем взаимодействует с оксидами железа с образованием силикатов железа:
(SiO2) + 2 (FeO) = (FeO)2 • SiO2 (204)
В дальнейшем по мере разложения известняка шлак обогащается СаО и образуются силикаты кальция:
(FeO)2 • SiO2 + 2(CaO) = (CaO)2 • SiO2 + 2(FeO). (205)
Кремнезем полностью связывается в силикаты кальция, и реакцию окисления кремния в условиях основной мартеновской печи следует считать необратимой.
Поведение марганца
Окисление марганца может проходить растворенным в металле кислородом, а также на границе со шлаком по реакции
[Mn] + (FeO) = [Fe] + (MnO). (206)
Постоянная равновесия определяется выражением
![]() (207)
(207)
Значение KMn с повышением температуры снижается. Поэтому в условиях мартеновской ванны марганец окисляется в начальные стадии процесса при относительно низких температурах. К концу доводки, когда температура ванны возрастает до 1580—1600° О, и при достаточно высоком содержании MnO в шлаке марганец восстанавливается из шлака. Восстановителем марганца, кроме железа, является углерод:
(MnO) + [Fe] = (FeO) + [Mn]; (208)
(MnO) + [С] = (СО) + [Mn]. (209)
Восстановление марганца к концу периода чистого кипения обычно наблюдается при его содержании в чугуне >1%. Марганец окисляется раньше железа и, связывая кремнезем в силикаты марганца, улучшает шлакообразование на ранних стадиях процесса.
Окисление и поведение фосфора
Реакция окисления фосфора экзотермическая и поэтому начинает протекать уже при относительно низкой температуре:
2 [Р] + 5 (FeО) = (Р2O5) + 5 [Fe]. (210)
В свободном состоянии Р2О5 в шлаке существовать не может, так как этот оксид неустойчив при высоких температурах. В период плавления Р2О5 преимущественно связывается в трифосфаты железа:
(P2O5) + 3(FeO) = (FeO)3 • P2O5. (211)
Во время спуска шлака в период плавления фосфор удаляется из ванны в виде этого соединения, при этом теряется и значительное количество железа.
В конце плавления и в последующие периоды плавки, когда шлак обогащается СаО, этот оксид играет основную дефосфорирующую роль. Наиболее прочными фосфатами кальция являются (СаО)3 • Р2O5 и (СаО)4 • P2O5.
В мартеновской печи в наибольшей степени, чем в каком-либо другом сталеплавильном агрегате, применяется дефосфорация металла путем многократного обновления шлака. Именно такая операция и проводится в период рудного кипения.
Фосфор в мартеновской печи преимущественно окисляется в период плавления и рудного кипения. В период чистого кипения для того, чтобы сдерживать восстановление фосфора из шлака в металл, необходимо сохранять высокую основность шлака. В период раскисления, когда в металл вносится кремний, основность шлака снижается. Основность уменьшается также при выдержке металла в ковше, поскольку протекает процесс частичного растворения футеровки, ковша и обогащения шлака кремнеземом. Это приводит иногда к рефосфорации и повышению содержания фосфора в металле к концу разливки на ≥0,005%. В связи с этим при выплавке низкофосфористой стали необходимо проводить глубокую дефосфорацию металла на ранних стадиях плавки и устранить восстановление фосфора в ковше, увеличивая вязкость шлака присадкой доломита и т. д.
Десульфурация металла
Сера в мартеновскую ванну вносится различными материалами: металлическим ломом, известняком, железной рудой и т. д. Однако основным источником серы является чугун, а при отоплении печи сернистым топливом, например мазутом, топливо также становится источником серы.
Десульфурация металла в условиях мартеновской печи осуществляется в основном, в результате перевода серы в прочные сульфиды, нерастворимые в металле. Сульфиды железа и марганца (FeS и MnS) растворимы в металле и шлаке. Однако сульфид марганца характеризуется значительно меньшей растворимостью в металле, чем сульфид железа. Поэтому при относительно высоком содержании марганца в металле протекает реакция
[FeS] + [Mn] = (MnS) + [Fe]. (212)
Константа равновесия этой реакции, поскольку содержание серы прямо пропорционально содержанию FeS, определяется выражением
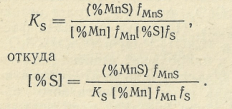
Константа равновесия КS возрастает с понижением температуры. Поэтому эффективная десульфурация металла возможна при высоком содержании марганца в металле, низком содержании сульфида марганца в шлаке и при относительной низкой температуре. Реакция (212) получает некоторое развитие в миксере. Заметное снижение содержания серы в чугуне наблюдается при периодическом скачивании шлака из миксера.
В значительно меньшей степени происходит десульфурация металла за счет марганца в мартеновской ванне в связи с относительно низким содержанием марганца, с одной стороны, и более высокой температурой металла, с другой. Основными реакциями процесса десульфурации в условиях мартеновской ванны являются следующие:
1) переход серы и одновременно железа из металла в шлак:
[Fe]+[S] = (Fe2+) + (S2-), (215)
или в молекулярной форме
[FeS] = (FeS); (216)
2) реакция в шлаковой фазе:
(FeS) + (CaO) = (CaS) + (FeO). (217)
Суммарная реакция десульфурации имеет вид:
[FeS] + (CaO) = (CaS) + (FeO). (218)
Переход серы из металла в шлак является диффузионным процессом и протекает медленно. Для его ускорения необходимо увеличивать скорость массопереноса в шлаке и поверхность контакта металла со шлаком, уменьшать вязкость шлака и металла. С повышением температуры вязкость металла и шлака уменьшается, возрастает скорость массопереноса. Вместе с тем повышенная температура затрудняет протекание реакции (218). Однако лимитирующим звеном процесса десульфурации металла в целом является диффузионная стадия. Поэтому процесс десульфурации ускоряется с повышением температуры. Постоянная равновесия реакции (218) определяется выражением
![]()
а коэффициент распределения серы между шлаком и металлом
![]()
Из анализа выражений (219) и (220) можно заключить, что удаление серы из металла протекает тем успешнее, чем выше содержание CaO и ниже содержание FeO в шлаке.
Однако, FeO уменьшает вязкость шлака, ускоряет процесс растворения извести в шлаке. Кроме того, часть серы в шлаке находится в виде FeS. Поэтому при содержании в шлаке 5—10% FeO и более, что характерно для мартеновского процесca, FeO, оказывая двоякое влияние на поведение серы, практически не влияет на процесс десульфурации.
В целом мартеновская печь не приспособлена для выплавки низкосернистого металла. Поэтому в случае необходимости получения стали с содержанием серы <0,025% необходимо прибегать к обработке металла синтетическим известково-глиноземистым шлаком.
Окисление углерода
Процесс окисления углерода в мартеновской печи состоит из следующих стадий:
- перехода кислорода из шлака в металл: (FeO) = [FeO]; (221)
- переноса кислорода и углерода к месту протекания реакции;
- взаимодействия углерода и кислорода: [С] + [O] = {СО}; (222)
- образования пузырей СО и их удаления из металла.
Самая медленная из указанных стадий будет ограничивать протекание процесса окисления углерода в целом. Наиболее быстрой является третья стадия, не лимитирующая процесс окисления углерода. Скорости перехода кислорода через границу раздела шлак-металл и переноса кислорода и углерода в металле определяются степенью перемешивания и заметно возрастают при непосредственном введении кислорода в металл. Поэтому скорость окисления углерода возрастает при продувке ванны кислородом.
Для образования пузырька СО в объеме металла необходимо преодолеть давление металла, шлака и газовой атмосферы печи, а также силы взаимодействия между частицами металла. Для преодоления этих сопротивлений затрачивается относительно много энергии, и поэтому пузырьки СО легче зарождаются на шероховатой поверхности подины, откосов и твердых неметаллических включений. Образовавшийся на поверхности подины или откосов пузырек СО, достигнув определенного объема, отрывается и поднимается вверх, что обеспечивает хорошее перемешивание ванны.
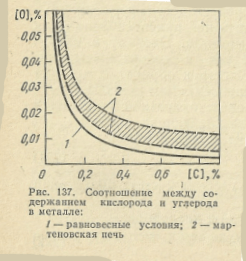
Для зарождения пузырька СО необходимо некоторое перенасыщение кислорода над равновесным его содержанием при данной температуре и данном содержании углерода. Поэтому содержание кислорода в металле мартеновской ванны несколько выше равновесного содержания с углеродом. Поскольку в период чистого кипения основной примесью в металле является углерод, то содержание кислорода в кипящей мартеновской ванне однозначно определяется концентрацией углерода (рис. 137).
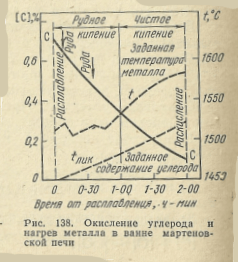
Основным требованием технологии ведения мартеновского процесса является соответствие между скоростями окисления углерода и нагрева ванны (рис. 138). К моменту окончания периода чистого кипения содержание углерода и температура металла должны достигнуть определенных значений. Поскольку при продувке ванны кислородом ускоряется нагрев металла и одновременно возрастает скорость окисления углерода, то широкое использование кислорода в мартеновских печах обеспечивает сокращение длительности плавок и повышение технико-экономических показателей работа мартеновских печей в делом.
Характер изменения состава металла и шлака по ходу плавки
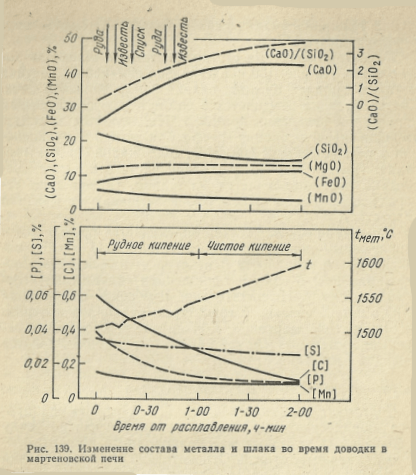
На рис. 139 представлено изменение состава металла и шлака по ходу плавки в мартеновской печи. Состав металла изменяется в соответствии с описанным характером поведения примесей. Наблюдается заметное уменьшение содержания фосфора к моменту раскисления и незначительное снижение содержания серы и марганца. Причем марганец в конце чистого кипения несколько восстанавливается из шлака. Содержание углерода непрерывно снижается, а температура металла возрастает.
Изменение состава шлака определяется прежде всего непрерывным повышением содержания CaO, а следовательно, и его основности и некоторым повышением содержания FeO в связи со снижением содержания углерода в металле. Незначительное изменение содержания MnO в шлаке связано с характером реакции окисления — восстановления марганца. Концентрация кремнезема непрерывно уменьшается, так как весь кремний окисляется в период плавления.