Типы систем принято классифицировать как гомогенные или однофазные, и гетерогенные, в которых содержится несколько фаз. Фазой называют часть системы, имеющей однородный состав, аналогичные физические и химические свойства в момент отсутствия внешних воздействий. В объеме системы фаза может присутствовать в замкнутой области, или разделяться на множество частей.
При этом, «фаза» и «агрегатное состояние вещества» не аналогичны, поскольку в системе могут быть фазы в одном агрегатном состоянии. В равновесной системе число фаз фиксировано, а при нагреве может изменяться.
Что такое фазы Гиббса

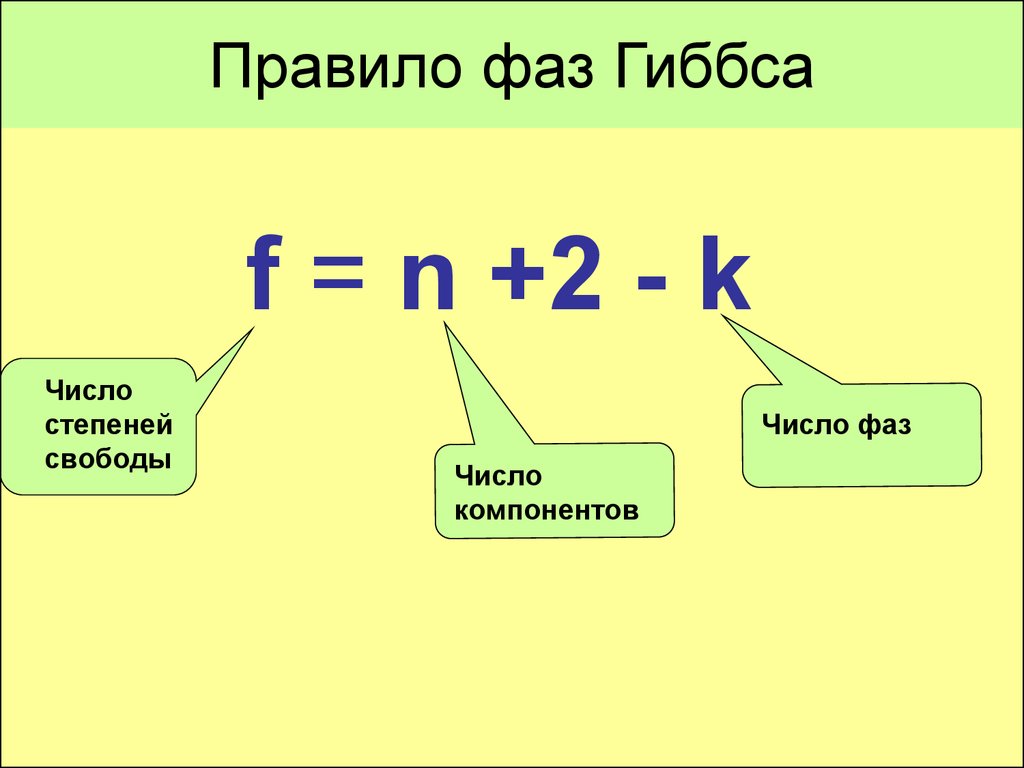
Основной закон равновесия фаз или правила фаз Гиббса определяет взаимосвязь количества фаз в системе Ф, компонентов К, степеней свободы С. Он отражает возможные варианты изменения внешних факторов, таких как:
- давление;
- температура;
- состав фаз — без изменения количества фаз в системе и выражается формулой: С = К — Ф + n, где n — определяется как количество внешних воздействий, влияющих на показатель равновесия системы.
Рассматривая сплавы, находящиеся под воздействием атмосферных условий, как правило, остается лишь один, температурный фактор, в связи с чем уравнение трансформируется, и выглядит следующим образом:
С = К — Ф + 1.
С — это сумма нескольких независимых переменных, описывающих состояние системы.
Для примера возьмем чистый металл. В процессе плавления число фаз в нем равно двум — это расплав и кристаллы, компонентов — 1, при этом степеней свободы — 0. Следовательно, в этот период воздействовать на внешние факторы (в нашем случае это температура), и менять их без изменения числа фаз в системе нельзя. Повышая температуру, мы получим одну фазу — расплав, понижая, также одну — кристаллы. Согласно правилу фаз Гиббса, получается, что однокомпонентная система поддерживает равновесие двух фаз, а двухкомпонентная — трех.
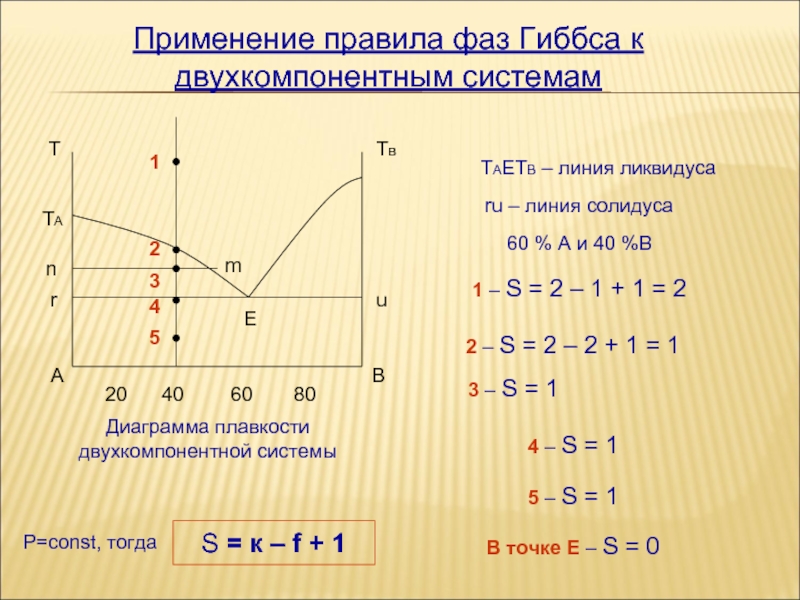
Построение диаграмм состояния
Правило фаз Гиббса и его применение актуально в ряде отраслей, в том числе и в металлургии, где оно используется при построении кривых нагрева и охлаждения металлов в процессе плавления. Один из способов создания диаграмм состояния — фиксация кривых охлаждения относительно температуры среды и времени при плавном ее охлаждении. При этом точки перегиба, отмеченные на кривых охлаждения в диаграмме, аналогичны точкам трансформаций фазового состава.

Построение диаграммы происходит в координатах:
- состав (в процентном соотношении А и В);
- температура в градусах Цельсия.
То есть, каждая зафиксированная на диаграмме точка показывает, в каком состоянии находится сплав определенного состава при воздействии данной температуры. Рассматривая основные типы диаграмм, можно увидеть следующую закономерность: растворяемость друг в друге компонентов, находящихся в жидком состоянии, не ограничена.
Итак, согласно правилу Гиббса в материаловедении, при ограничениях параметров состояния среды, число степеней свободы сокращается в соответствии с количеством ограничений.