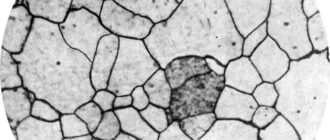
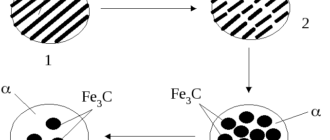
Подавляющее большинство реакций растворения сопровождается выделением либо поглощением тепла с попутным изменением объема получаемого раствора. Это является следствием двух процессов — разрушением структуры вещества, которое растворяется, и его взаимодействия с растворителем.
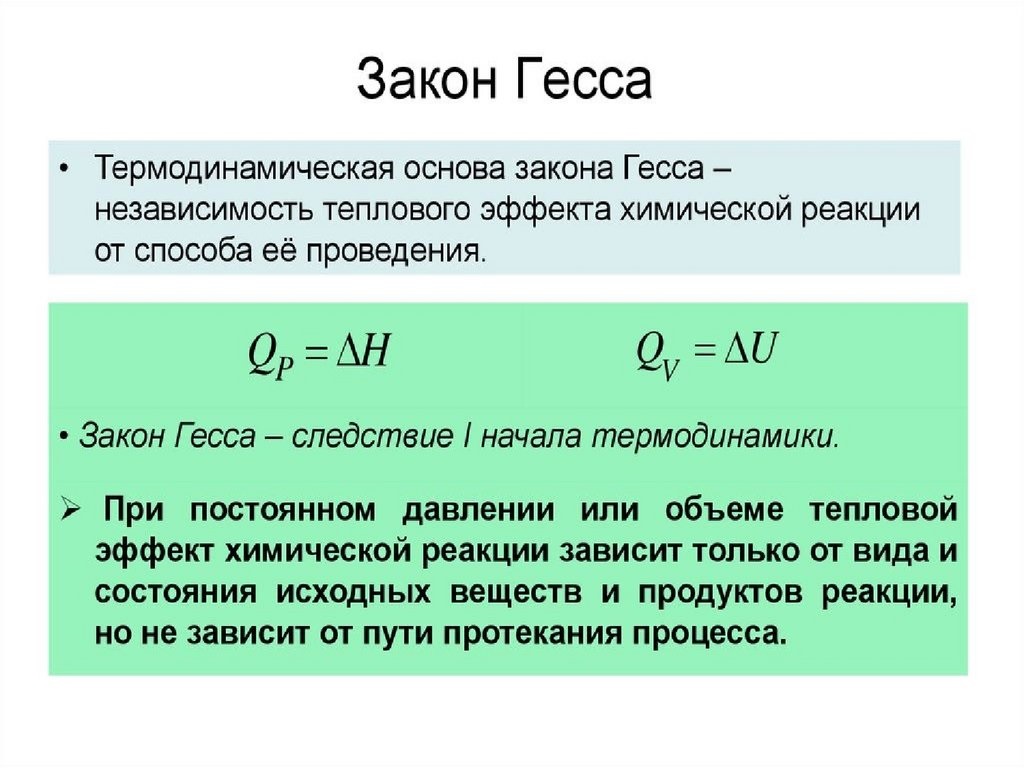
Закон Гесса
Г. И. Гесс — русский ученый швейцарского происхождения, один из основателей термохимии, сформировал закон, получивший его имя. Его формулировка утверждает, что тепловой эффект любой химической реакции не зависит от ее промежуточных этапов, т.е. определяется начальным и конечным состоянием системы. Действие закона Гесса распространяется на расчеты тепловых эффектов, происходящих при стандартных условиях, которыми являются:
- давление — 1 атм=10 Па;
- температура — 273К+25=298К.

Значения теплоты для реакций различных компонентов сведены в справочную таблицу. Расчет теплового эффекта реакции осуществляется вычитанием суммы теплоты, образовавшейся в исходных веществах. При условной реакции типа аА +bВ = сС + dD тепловой эффект рассчитывается по формуле: ΔН°=(cΔН°обр.С+dΔН°обр.D)-(aΔН°обр.А+bΔН°обр.В). Для части материалов, например, С, Н2, Fe это значение изначально равно нулю.
Согласно этому выведены два следствия из вышеприведенного закона:
- Энтальпия формирования 1 моля при реакции простых веществ не определяется способом его получения.
- Теплота происходящей реакции является суммой теплоты сгорания исходных реагентов за минусом этого показателя по отношению к компонентам с применением коэффициентов стехиометрии.
Суть теплового эффекта в растворах
Интенсивность реакций, сопровождающих тепловой эффект растворения, зависит от строения реагентов и их химической активности. Например, растворяя в воде серную кислоту, можно наблюдать экзотермическую реакцию, т.е. выделение значительного количества тепла, что также наблюдается при введении в воду сернокислой меди. Эндотермия, или резкое понижение температуры раствора, происходит в водных растворах азотнокислого калия и аммония. А вот раствор воды и натрия хлористого остается стабильным, и практически не изменяется в ходе процесса.
Итак, выделение тепла в ходе химической реакции — это изменение энтальпии и внутренней энергии, являющейся следствием трансформации реактантов в объемах, соответствующих стехиометрии процесса при создании следующих условий:
- одинаковой температуре исходных реагентов;
- работа против внешнего давления.

Тепловой эффект растворения используется в металлургических технологиях при расплавлении руд для получения металлов — алюминия, меди и пр. Этот показатель важен для качества сплавов и определяется с помощью тигля, разделенного горизонтальной перегородкой с отверстием. Его помещают в печь, предварительно загрузив в нижнюю и верхнюю часть компоненты сплава, и закрыв отверстие в перегородке. После нагрева до определенной температуры заглушка убирается, происходит смешивание слоев, затем производятся замеры температуры растворения.