В течение плавки стали в дуговой печи кислород попадает в металл и частично растворяется в нем, такой процесс обычно называют окислением металла.
Окисление металла и его примесей происходит в основном за счет оксидов железа, загруженных на шлак твердых окислителей, вдуваемого в печь и в расплав газообразного кислорода и в незначительной степени за счет кислорода печной атмосферы. Присадки твердых окислителей на шлак приводят к повышению содержания в нем оксидов железа (Fe2O3, FeO). На границе раздела металл — шлак Fe2О3 восстанавливается до FeО. В соответствии с законом распределения кислород переходит из шлака в металл по схеме
(FеО) = [Fе] + [О].
Оксиды железа могут передавать в металл кислород из печной атмосферы, в том числе и в случае подачи кислорода в рабочее пространство, когда на поверхности контакта шлака и печной атмосферы FеО окисляется до Fе2O3 по схеме
2(FеО) — 1/2 O2=(Fе2O3).
Образовавшийся оксид Fе2O3 восстанавливается на поверхности контакта с металлом до FеО, что способствует переходу кислорода в металл вследствие увеличения концентрации и активности FеО и повышения окислительной способности шлака. Кислород, поступивший в расплав, расходуется в основном на окисление примесей.
При вдувании газообразного кислорода непосредственно в металлический расплав струя кислорода внедряется в металл, и в этой зоне, по-разному называемой в специальной литературе (зона продувки, зона внедрения, реакционная зона), на поверхности пузырьков и струй идет прямое окисление железа по схеме
2[Fе] + O2газ=2(FеО).
Там же может протекать окисление примесей кислородом:
[С] + 1/2 O2газ=СО; 2[Мn] + O2газ =2(МnО);
[Si] + O2газ = (SiO2) и т.д.
Объем зоны продувки сравнительно невелик, даже в кислородных конверторах он не превышает 10… 13 %. Поэтому окисление примесей в основном протекает в остальном объеме ванны, часто называемом циркуляционной зоной. Кислород туда попадает вследствие растворения его в железе в зоне продувки по схеме (FеО) = Fе + [О] и последующего переноса в объеме расплава конвективными потоками.
Следует помнить, что часть примесей, находящихся в металлическом расплаве, легко окисляется кислородом (Si, Тi, Аl, V, В); часть примесей практически не окисляется (Ni, Мо, Сu, Со, W); часть примесей окисляется не полностью (Мn, Сr).
Наибольший интерес для металлургов представляет реакция окисления углерода, так как продуктом этой реакции является газообразный оксид углерода СО , пузырьки которого, выделяясь из металлического расплава, перемешивают его, способствуют выравниванию химического состава расплава и его температуры, ускоряют нагрев металла, удаляют растворенные в металле газы, проходя через слой шлака, способствуют его вспениванию.
Процесс окисления углерода в ванне сталеплавильной печи достаточно хорошо изучен и может быть описан следующими схемами:
1) окисление кислородом оксидов железа шлака
[С] + (FеО)ж = Fеж + СОгаз;
2) окисление кислородом, растворенным в металле,
[С] + [O] → СOгаз;
3) окисление газообразным кислородом в виде пузырьков, попавших в ванну при продувке кислородом,
[С] + 1/2 O2газ → СОгаз .
Повышение температуры всегда способствует более полному и быстрому окислению углерода. Заметное окисление углерода наблюдается лишь при определенной температуре. Минимальный необходимый перегрев металла над линией ликвидуса (температурой полного расплавления), при котором начинается процесс окисления углерода, составляет 30…40 °С, практически он несколько выше.
Следует помнить, что при окислении углерода газообразным кислородом суммарный тепловой эффект процесса положителен и выделяется большое количество тепла; при окислении углерода оксидами железа шлака суммарный тепловой эффект процесса отрицательный из-за больших затрат энергии на перенос кислорода из шлака и тепло поглощается ванной. Поэтому окисление углерода газообразным кислородом в принципе начинается раньше и может быть использовано, как отмечалось выше, для ускорения расплавления ванны. При окислении углерода оксидами железа шлака, вносимыми в шлак твердыми окислителями, температура ванны сначала может снизиться, так как тепло расходуется на нагрев и плавление твердых окислителей, а затем— на осуществление реакции окисления углерода оксидами железа шлака, соответственно уменьшится и скорость окисления углерода. Практически с самого начала применения газообразного кислорода в металлургии даже в старых цехах с маломощными печами стремились проводить комбинированное окисление углерода твердыми окислителями и газообразным кислородом для ускорения процесса.
При изучении кинетики процесса обезуглероживания многочисленными исследованиями были установлены так называемые критические концентрации углерода (0,15…0,30 %), при достижении которых резко снижается скорость окисления углерода и изменяется режим взаимодействия углерода и кислорода. В области концентраций углерода выше критических процесс окисления углерода лимитируется внешней диффузией (интенсивностью подачи кислорода), т. е. увеличив интенсивность подачи кислорода в расплав, можно увеличить и скорость реакции окисления. При концентрации углерода ниже критических скорость обезуглероживания почти не зависит от интенсивности продувки кислородом и уменьшается пропорционально понижению концентрации углерода. При концентрациях углерода менее 0,05 % скорость обезуглероживания определяется только диффузией углерода к месту протекания реакции и может быть повышена лишь за счет дополнительного перемешивания расплава.
В отдельных случаях скорость процесса обезуглероживания может определяться процессом выделения СО, получаемого в результате окисления углерода. Известно, что для образования пузырька СО в металле необходимо преодолеть давление столба металла рм, столба шлака рш, атмосферы над ними ратм, силы сцепления жидкости 2 σ/r, где σ — поверхностное натяжение металла, r — радиус образующегося пузырька:
РвыдCO ≥ Рм + Рш + Ратм + 2 σ/r
При малых значениях r величина 2 σ/r огромна и образование пузырьков СО в объеме жидкого металла практически невозможно. Такой процесс возможен лишь на границах раздела фаз: шлак — металл; неметаллическое включение — металл; футеровка ванны — металл; газовый пузырь -металл. Наиболее благоприятны условия образования пузырьков СО на границе раздела футеровка — металл, вследствие шероховатости футеровки, плохой смачиваемости ее металлом и наличия микропор, заполненных воздухом, в поверхностном слое футеровки.
Наблюдаемая в конце окислительного периода плавки окисленность металла близка к равновесной для реакции окисления углерода, но несколько выше ее (рис. 3.1). Разница между фактической и равновесной концентрациями углерода вызвана как раз трудностями с выделением оксида углерода (СО) в газовую фазу.
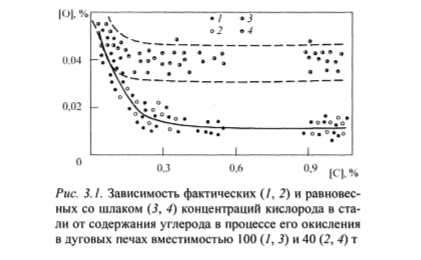
Следует подчеркнуть, что для условий окислительного периода плавки вполне допустимо окисленность металла характеризовать содержанием кислорода в металле, определенном методом вакуум- плавки. Как известно, этот метод позволяет определить лишь общее содержание кислорода в металле
[O]общ = [O]раств + [O]включ
В окислительный период плавки в результате кипения ванны практически все кислородсодержащие неметаллические включения из ванны удаляются и [О]общ = [О]раств, т. е. весь кислород растворен в металле. В дальнейшем после раскисления стали в ней содержится некоторое количество неметаллических продуктов раскисления и часть кислорода находится в виде [О]вкл . Из-за трудностей определения содержания растворенного в металле кислорода окисленность металла в таких случаях обычно характеризуют величиной активности кислорода в металле , получаемой расчетным путем с учетом состава стали либо определяемой методом ЭДС непосредственно в жидком металле.




