Свойства никеля
Никель относится к переходным металлам первого длинного периода и в периодической системе Д.И. Менделеева располагается в VIIIA подгруппе вместе с железом и кобальтом.
Никель кристаллизуется в кубической гранецентрированной решетке с периодом при комнатной температуре, равным 0,352387 нм. Атомный диаметр никеля – 0,248 нм. Плотность никеля (8,897 г/см3) почти такая же, как у меди, и в два раза превышает плотность титана, так что никель относят к числу тяжелых цветных металлов.
Физические свойства никеля приведены в табл. 7. Скрытая теплота плавления никеля примерно такая же, как у магния, и несколько больше, чем у алюминия. Его удельная теплоемкость сравнительно невелика и лишь немного превышает теплоемкость меди. Удельная электро- и теплопроводность никеля меньше, чем у меди и алюминия, но значительно превышает электро- и теплопроводность титана и многих других переходных металлов. Модули упругости у никеля примерно такие же, как у железа.

Никель – ферромагнитный металл, но его ферромагнетизм выражен значительно меньше, чем у железа и кобальта. Точка Кюри для никеля составляет 358 ˚С, выше этой температуры никель переходит в парамагнитное состояние.
Чистый никель – металл серебристого цвета. При высокотемпературном окислении никеля образуются два оксидных слоя: внутренний – светло-зеленый и внешний – темно-зеленый. Два этих слоя состоят из оксида, но отличаются количеством кислорода.
Никель характеризуется более высокой коррозионной стойкостью в атмосферных условиях по сравнению с другими техническими металлами, что обусловлено образованием на его поверхности тонкой и прочной защитной пленки. Никель обладает достаточной устойчивостью не только в пресной, но и в морской воде. Минеральные кислоты, особенно азотная, сильно действуют на никель. Щелочные и нейтральные растворы солей на никель влияют незначительно даже при нагревании, в кислых растворах солей он корродирует довольно сильно. В концентрированных растворах щелочей никель устойчив даже при высоких температурах.
Никель при комнатной температуре не взаимодействует с сухими газами, но присутствие влаги заметно повышает скорость его коррозии в этих средах. Никель, загрязненный кислородом, склонен к водородной болезни.
Сырье для получения никеля
В настоящее время никелевые заводы перерабатывают в основном два типа руд, резко различающихся по химическому составу и свойствам: окисленные никелевые и сульфидные медно-никелевые. Значение этих руд для отечественной никелевой промышленности и за рубежом различно. В России из года в год возрастает доля никеля, получаемого из сульфидных руд, а в зарубежных странах, наоборот, все большее значение приобретают окисленные руды.
Окисленные никелевые руды представляют собой горные породы вторичного происхождения, состоящие в основном из гидратированных магнезиальных силикатов, алюмосиликатов и оксида железа. Никелевые минералы в них составляют незначительную часть рудной массы. Наиболее часто никель находится в виде бунзеита (NiO), гарниерита [(Ni, Mg)O · SiO3 · nH2O] или ревденскита [3(Ni, Mg)O · 2SiO2 · 2H2O]. Кроме никеля полезным компонентом этих руд является кобальт, содержание которого обычно в 15…25 раз меньше содержания никеля. Иногда в окисленных рудах присутствует в небольших количествах медь (0,01…0,02 %).
Пустая порода, составляющая основную массу руды, представлена глиной Al2O3 · 2SiO2 · 2H2O, тальком 3MgO · 4SiO2 · 2H2O, другими силикатами, бурым железняком Fe2O3 · nH2O, кварцем и известняком.
Окисленные никелевые руды отличаются исключительным непостоянством состава по содержанию как ценных компонентов, так и пустой породы. Эти колебания состава наблюдаются даже в массиве одного месторождения. Возможные пределы концентраций компонентов руды характеризуются следующими цифрами, %: Ni – 0,7…4; Co – 0,04…0,16; SiO2 – 15…75; Fe2O3 – 5…65; Al2O3 – 2…25; Cr2O3 – 1…4; MgO – 2…25; CaO – 0,5…2; конституционная влага – до 10…15.
По внешнему виду окисленные никелевые руды похожи на глину. Для них характерны пористое, рыхлое строение, малая прочность кусков, высокая гигроскопичность. Рациональных методов обогащения таких руд до сих пор не найдено, и они после соответствующей подготовки непосредственно поступают в металлургическую переработку.
В сульфидных рудах никель присутствует главным образом в виде пентландида, представляющего изоморфную смесь сульфидов никеля и железа переменного соотношения, и частично в форме твердого раствора в пирротине.
Основным спутником никеля в сульфидных рудах является медь, содержащаяся главным образом в халькопирите. Из-за высокого содержания меди эти руды называют медно-никелевыми. Кроме никеля и меди в них обязательно присутствуют кобальт, металлы платиновой группы, золото, серебро, селен и теллур, а также сера и железо. Таким образом, сульфидные медно-никелевые руды являются полиметаллическим сырьем очень сложного химического состава. При их металлургической переработке в настоящее время извлекают 14 ценных компонентов.
Химический состав сульфидных медно-никелевых руд следующий, %: Ni – 0,3…5,5; Cu – 0,2…1,9; Co – 0,02…0,2; Fe – 30…40; S – 17…28; SiO2 – 10…30; MgO – 1…10; Al2O3 – 5…8. По структуре медно-никелевые руды могут быть сплошными, жильными и вкрапленными. Чаще встречаются два последних типа руд. В зависимости от глубины залегания руду добывают как открытым, так и подземным способом.
В отличие от окисленных никелевых руд медно-никелевые руды характеризуются высокой механической прочностью, негигроскопичны и могут подвергаться обогащению.
Основным способом обогащения сульфидных медно-никелевых руд является флотация. Иногда флотационному обогащению предшествует магнитная сепарация, направленная на выделение пирротина в самостоятельный концентрат. Возможность проведения магнитной сепарации обусловлена относительно высокой магнитной восприимчивостью пирротина.
Выделение пирротинового концентрата при обогащении руды улучшает качество первичного никелевого концентрата вследствие вывода из него значительной части железа и серы и упрощает его последующую металлургическую переработку. Однако при получении пирротинового концентрата возникает необходимость в обязательной его переработке с целью извлечения никеля, серы и платиноидов.
Флотационное обогащение медно-никелевых руд может быть коллективным или селективным. При коллективной флотации за счет отделения пустой породы получают медно-никелевый концентрат. Однако и селективная флотация не обеспечивает полного разделения меди и никеля. Продуктами селекции в этом случае будут медный концентрат с относительно небольшим содержанием никеля и никелево-медный концентрат, отличающийся от руды более высоким отношением Ni : Cu.
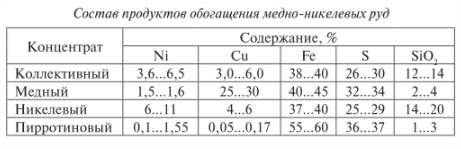
Таким образом, в зависимости от принятой схемы обогащения сульфидных медно-никелевых руд можно получать коллективные медно-никелевые, медные, никелевые и пирротиновые концентраты, состав которых приведен в табл. 8.
Способы получения никеля
Сульфидные руды и окисленные руды перерабатывают различными способами – пиро- и гидрометаллургическими.
Плавка на штейн сульфидных руд и концентратов
Руды с суммарным содержанием больше 2–5 % меди и никеля считают богатыми, их плавят без предварительного обогащения.
Руды и концентраты содержат одни и те же минералы, поэтому к ним могут быть применены после необходимой подготовки одни и те же способы переработки.
При нагревании руды до 400–600 ˚С еще до начала плавления халькопирит и никельсодержащие сульфиды разлагаются:
6(NiS, FeS) → 2Ni3S2 + 6FeS + S2 ,
4CuFeS2 → 2Cu2S + 4FeS + S2 ,
2Fe7S8 → 14FeS + S2 .
В результате этих реакций сложная совокупность минералов превращается в смесь простых сульфидов: Ni3S2 , FeS и Cu2S.
При температурах, необходимых для плавления шлака, состоящего из окислов пустой породы и флюсов, сульфиды меди, никеля и железа неограниченно растворимы друг в друге; они образуют медно-никелевый штейн, отделяемый от шлака в виде более тяжелого жидкого слоя.
Если часть серы при плавке окислена или удалена предварительным обжигом, распределение меди, никеля и железа между штейном и шлаком будет зависеть от сродства этих металлов к кислороду и сере. В условиях плавки сродство к сере, определяющее возможность перехода металла в штейн, у меди больше, чем у никеля, а у никеля больше, чем у железа. Сродство тех же металлов к кислороду убывает в обратной последовательности. При недостатке серы для сульфидирования всех металлов сначала будет переходить в штейн медь, затем никель и, наконец, часть железа. Чем больше железа перейдет в штейн, тем больше полнота сульфидирования меди и никеля, но штейн, разбавленный сернистым железом, будет бедным. Для полного перевода никеля в штейн при плавке руды или концентрата не стремятся к полному шлакованию железа, оставляя часть его в штейне.
Кобальт по сродству к сере и кислороду занимает промежуточное положение между железом и никелем.
Расплавленный штейн продувают в конвертере, добавляя кварц; железо, окисляясь, шлакуется кремнеземом.
Основной продукт конвертерного передела – медно-никелевый файнштейн – представляет собой сплав сульфидов меди и никеля, содержащий 1–3 % железа.
Кобальт при продувке частично шлакуется вместе с железом.
Конвертерный шлак иногда направляют в отдельный передел для извлечения кобальта. Благородные металлы концентрируются почти полностью в файнштейне.
Охлажденный файнштейн дробят, измельчают и подвергают флотации. При этом получают два концентрата: никелевый, состоящий почти из чистого Ni3S2 , и медный, содержащий Cu2S; последний перерабатывают на медь обычным медным концентратом плавкой на штейн и продувкой в конвертере.
Никелевый концентрат обжигают, окисляя его по реакции
2Ni3S2 + 7O2 = 6NiO + 4SO2 .
Полученный таким образом серый порошок закиси никеля, содержащий окислы кобальта и платиновые металлы, восстанавливают углем в электропечах до металла, который разливают в аноды.
Никелевые аноды подвергают электролитическому рафинированию, попутно извлекая из электролита кобальт и остаток меди, а из шлама – платиноиды.
Богатые крупнокусковые медно-никелевые руды плавят на штейн в шахтных печах, если пустая порода этих руд не слишком тугоплавка. В ряде случаев для руд, содержащих много окиси магния или другие тугоплавкие составляющие, приходится прибегать к электроплавке.
Флотационные концентраты и мелкие фракции богатых руд плавят в отражательных или электрических печах; при высоком содержании серы в этих материалах применяют предварительный обжиг.
Выбор способа плавки во многом зависит от состава сырья и местных экономических условий, в частности от наличия того или иного топлива и цены на электроэнергию.
Гидрометаллургический способ переработки сульфидных руд
По этому способу измельченную руду или концентрат обрабатывают раствором аммиака и (NH4)2SO4 в автоклавах под избыточным давлением воздуха около 506,7 кн/м2 (7ат). Медь, никель и кобальт переходят в раствор в виде комплексных аммиачных солей, например по реакции
NiS + 2O2 + 6NH3 = Ni(NH3)6SO4 .
Энергичное окисление сульфидов сопровождается выделением тепла, избыток которого отводят холодильниками, поддерживая в автоклаве температуру 70–80 ºС, сера, входящая в состав концентрата, при этом окисляется до S2O32−, S3O62−и SO42− , а железо выпадает в осадок в виде гидроокиси и основных сульфатов.
Отфильтрованный раствор кипятят для осаждения меди по реакции
Cu2+ + 2S2O32− = CuS + SO42− + S + SO2 .
После этого частично оставшуюся в растворе медь осаждают сероводородом, а очищенный от нее раствор, содержащий никель и кобальт, обрабатывают в автоклаве водородом при давлении около 2,5 Мн/м2 (25 ат) и температуре около 200 ºС.
Сначала осаждается основная масса никеля
Ni(NH3)62+ + H2 = Ni + 2NH4+ + 4NH3
в виде частиц крупностью от 2 до 80 мкм. Отфильтровав осадок, остаток никеля и кобальт выделяют из раствора сероводородом.
При дальнейшей обработке осадка сульфидов кислородом и аммиаком в автоклаве растворяется кобальт. Нерастворимый осадок, содержащий преимущественно сульфид никеля, возвращают на основное выщелачивание, а из раствора действием водорода под давлением выделяют кобальт.
Схема сложна и требует дорогой аппаратуры; однако она позволяет извлекать из комплексных концентратов до 95 % Ni, около 90 % Сu и 50–75 % Со.
Плавка окисленных руд на штейн
Наиболее распространенный в настоящее время способ переработки окисленных никелевых руд плавкой на штейн основан на различии сродства железа и никеля к кислороду и сере.
Никель путем сульфидирования переводится в штейн – сплав Ni3S2 и FeS; основная масса железа удаляется со шлаком:
6FeS + 6NiO = 6FeO + 2Ni3S2 + S2 ,
2FeO + SiO2 = FeSiO4 .
Окисленные руды не содержат серы, поэтому ее приходится вводить, добавляя при плавке пирит или гипс. Гипс, восстанавливаясь до сернистого кальция, сульфидирует железо и никель. Действие гипса при плавке более сложно, чем действие пирита, однако во многих случаях все же пользуются гипсом, а не пиритом, так как гипс дешевле пирита и не дает
железистых шлаков.
Наиболее выгодно при переработке окисленных никелевых руд применять местный кобальтсодержащий пирит, в котором очень мало меди и нет благородных металлов.
Никелевый штейн, полученный в результате плавки руды с пиритом или гипсом, содержит до 60 % Fe, которое далее отделяют от никеля продувкой жидкого штейна в конвертере. При конвертировании происходит избирательное окисление железа и шлакование его добавляемым в конвертер кварцем – получается практически чистый от железа никелевый файнштейн. Конвертерный шлак богат никелем, поэтому он является оборотным продуктом – его возвращают в рудную плавку либо направляют на отдельную переработку для извлечения кобальта.
Файнштейн разливают в изложницы, затем измельчают и обжигают намертво:
2Ni3S2 + 7O2 = 6NiO + 4SO2 .
Закись никеля смешивают с малосернистым восстановителем, например с нефтяным коксом, и плавят в электрической печи при 1500 ºС, получая жидкий никель.
Никель отливают в аноды для электролитического рафинирования либо гранулируют, сливая его тонкой струей в воду.
Плавка окисленных руд на никелистый чугун (ферроникель)
Богатые окисленные руды иногда плавят в электрических печах с углем, восстанавливая из них все железо, никель и кобальт в природнолегированный чугун.
Подобную плавку сравнительно бедных руд проводят и в доменных печах, однако она имеет ограниченное применение.
Несмотря на преимущественное использование никеля в специальных сталях, выплавка его в виде сплава с железом не всегда приемлема: в сплав переходят кобальт, марганец, хром и другие примеси, случайные сочетания которых не всегда позволяют использовать ценные свойства этих металлов.
Кричный способ переработки окисленных руд
По этому способу руду, смешанную с углем, нагревают в трубчатых вращающихся печах при температуре около 1050 ºС, позволяющей восстановить вместе с никелем и кобальтом только часть железа. Восстановленные металлы получаются в виде зерен, смешанных с полурасплавленным шлаком. Охлажденный шлак дробят и извлекают из него кричный сплав электромагнитом. Способ не получил широкого распространения по тем же причинам, что и предыдущий, – из-за невозможности отдельного использования кобальта.
Гидрометаллургия окисленных руд
По одному из этих способов, известному в литературе под названием кубинского, измельченную руду подвергают восстановительному обжигу в механических многоподовых печах в среде генераторного газа. При 600–700 ºС никель и кобальт восстанавливаются до металлов, а железо – только до закиси. Далее руду выщелачивают раствором аммиака в присутствии углекислоты и кислорода воздуха. Никель образует растворимые в воде аммиакаты по реакции
2Ni + 12NH3 + 2CO2 + O2 = 2Ni(NH3)6CO3.
После отделения пустой породы сгущением и промывкой раствор обрабатывают острым паром. В результате удаления избытка аммиака протекает гидролиз с выделением в осадок основных карбонатов никеля:
2Ni(NH3)6CO3 + H2O = NiCO3Ni(OH)2 + CO2 + 12NH3 .
Аммиак из газов поглощают водой и вновь направляют на выщелачивание. Закись никеля спекают на агломерационных машинах и в виде спека поставляют на сталеплавильные заводы.
